準備問題集 日本語版(実験の部)
| 問題24 | フリーデル−クラフツ反応:1,4-ジ-tert-ブチル-2,5-ジメトキシベンゼンの合成 |
| 問題25 | マレイン酸の滴定 |
| 問題26 | 2,3-ジフェニルキノキサリンの調製 |
| 問題27 | 3-(4-メトキシフェニル)プロパン酸の合成:接触水素移動反応の例 |
| 問題28 | 錯滴定(キレート滴定) |
| 問題29 | N-アセチルアラニンの酵素による加水分解:環境に優しいプロセスの例 |
安全規則
これらの規則は化学オリンピックの国際判定基準で認められているものです。生徒たちはすべて,化学オリンピックに参加する前に,これらの規則をよく理解しておかねばならない。実験問題試験の実施前に,簡単に説明を受ける機会もあります。
1 与えられる指示を聞けるように常に注意を払っていて,その指示には注意して従うこと。常に真剣な態度でのぞむこと。異常事態が,いつ起こっても大丈夫なように覚悟しておくこと。消火器,安全シャワー,洗眼シャワーの位置を熟知し,また正しい使い方を学んでおくこと。実験操作,実験器具,薬品などについての質問がある場合には指導員(インストラクター)に尋ねること。
2 有害または異臭のする蒸気が発生する可能性がある実験はすべて,ドラフト内でおこなわなければならない。これらの化学反応をすみやかに停止させる手段を熟知しておくこと。
3 実験室内では常に,安全メガネ(横側にも防護シールドのついたもの)を着用のこと。コンタクトレンズを使用している者は,目全体を覆うことができる安全ゴーグルを着用しなければならない。目の事故を防ぐためには極力注意をはらわなければなりません。実験室への入室を許可する前に,インストラクターがすべての防護用器具が十分であるかをチェックします。自分の安全メガネを持ってくるよう,各国に既に通知がしてありますが,予備のメガネ類もいくつか用意してあります。
4 長袖で膝まである実験着と足の甲を覆うだけの靴を着用しなければなりません。サンダルなども使用禁止です。襟の下まである長髪は束ねること。自分の実験着,ヒールの低く,すべりにくい靴,髪を止めるピンなどをかならず持参してください。
5 実験室内での,飲食,喫煙,ガムを噛むことは厳禁です。
6 事故が起こったらすべて報告しなければなりません。化学の実験室では,不用意に薬品をこぼすこと,ガラスの破片,火気などは危険の要因となります。安全に実験をするコンディションを整えるための操作を学ぶことも,実験化学のトレーニングの一部です。特定の実験についての安全の指針は実験操作に関する注意書きに詳しく記載されています。
7 すべての化学薬品を,注意を払って取り扱わなければなりません。腐食性のもの,毒性の薬品などもあり,多くの薬品(特に有機物)は引火性です。初めて使用する薬品を取り扱うときには,つねに安全に関するPractical Task Paper にある注意書きを読むように心がけてください。
8 薬品は決して食べて(なめて)はいけません。また,ピペットを口で吸ってもいけません。つねに,ピペッターを利用してください。
9 薬品には不用意に接しないように心がけましょう。薬品が皮膚に触れてしまったときには,蛇口または安全シャワーの流水を少なくとも10分間は流し続けて洗い,それから応急処置をして医師の治療を受けるよう適切に対処してください。有機物は皮膚から吸収されやすいので,触れた場合には,1)流水で流し 2)石鹸で洗い 3)水ですすぎ 4)エチルアルコールですすぎ 5)再び石鹸で洗ってから 6)最後に水ですすいで下さい。薬品で汚れた衣服はすぐに脱ぎ,完全に洗うようにしましょう。
10 薬品が目に入ったら,すみやかに,洗顔器を用いて水で何度も洗ってください。適切な応急処置をしてから医師の治療を受けてください。
11 多くの化学薬品は引火性ですから,使用中は火気厳禁です。最寄の消火器,消火布,安全シャワーの位置を必ず知っていなければなりません。もしも人の衣服に火がついた場合には,その人を床の上に横にさせ回転させて炎を消させてください。近くに消火布か白衣があるときにはそれを利用してください。たとえ安全シャワーを使うときでも,火がついた人を立たせたり走らせたりすると炎が頭部に燃え移りますので絶対にしないでください。いかなる種類の化学消火器も人に向けて使ってはいけません。
12 あなたが実験している実験室内で火災が発生した場合には,近くの人やインストラクターに知らせるために「ファイアー(英語)」で叫んでください。試験管の中で発生したような小さな火は,ふつうは時計皿のような容器で口を塞げば消すことができます。もしも,一台の消火器または砂,水などで消すことができなかった場合には,逃げるように指示される(ので従って下さい)。
13 退避するときには次のことを守ってください。1)冷静を保つ 2)使用している火気を消す 3)電気のスイッチを切る。 開いている窓や近くのドア(室内)を閉めてください。最寄の非常口まですばやく歩き(ただし走ってはいけません),建物から出てください。あなたの名前が退避者リストに載っていて,行方不明者として扱われていないことを確認してください。
14 すべてのガラス器具は注意して取り扱ってください。ガラスは非常に硬いですが,引っ張りや曲げには脆い材料です。もし,折れたり破砕したときには,傷口のガラスの破片は取り除いておかなければなりません。壊れたガラス器具のすべての破片を担当のインストラクターに調べてもらってください。ガラス器具を壊したときは必ず報告して,清掃してください。また担当のインストラクターに申し出て代わりの器具と交換してください。
15 薬品の廃棄物は絶対に洗い流さないで下さい。化学薬品は一切,排水システムに出てはいけません。反応後の残留物の廃棄には説く鉄に注意を払ってください。重要であると思われる箇所には詳しい注意書きが書いてあり,特別な廃棄物用の瓶が用意されています。
16 自分に割り当てられた実験台はそれぞれ責任をもって下さい。薬品や水がこぼれたときにはすぐにふき取って下さい。高濃度の酸をこぼしたときには,まず炭酸水素ナトリウムを用いて中和し,大量の水で洗って下さい。自分の実験台の周りは常にきれいに保ってください。床にこぼした薬品はすぐに洗い流し,落として割ったガラス器具は掃き取って下さい。
17 実験が終わり実験室を出る前に,水,スチーム,ヒーター,ガス栓をすべて閉じて下さい。
実験問題解答に向けてのヒント
今年の実験問題試験ではマイクロスケール実験装置を使用します。化学オリンピックの実験問題において,このような装置を使用するのは初めてなので簡単に使用法の説明をしておきます。マイクロスケールガラス器具は,次に示すような内容でケースに収納されています。
薬品、ガラス器具および実験装置:
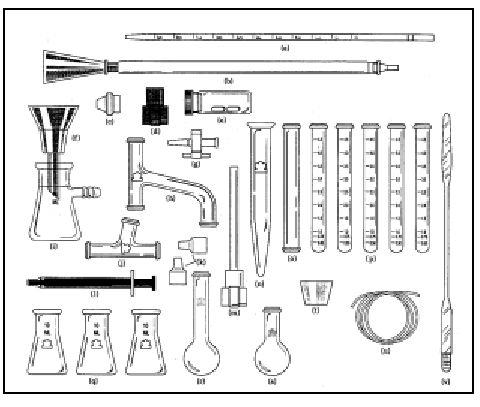
マイクロスケールガラス器具キットの内容
![]() (b)
クロマトグラフィー管
(b)
クロマトグラフィー管
(c) 温度計アダプター
(d) 温度計接合用器具
(e) 磁気攪拌子(二個入り)
(f) 吸引漏斗
(g) 二方コック
(h) 蒸留頭部60 mm
(i) 吸引フラスコ 25 mL
(j) 枝分れ管(ト字管)
(k) ゴムストッパー8 mm
(l) ポリエチレン製シリンジ1 mL
(m) 支持棒つきコネクタ
(n) 遠心分離用試験管15 mL
(o) 精留塔
(p) 反応用試験管10 x 100 mm
(q) 三角フラスコ10 mL
(r) 長首丸底フラスコ5 mL
(s) 丸底フラスコ5 mL
(t) 濾過用アダプタ
(u) テフロン製チューブ1/16”
(v) ミクロ薬さじ
重要なお知らせ
準備問題集のこのセクションで出てくる実験はすべて,どのような種類の小型のガラス器具を用いても行なうことができます。実際に実験をおこなうスケールは400 mg サイズです。実験問題試験の実施に先立ち,マイクロスケール実験装置を使った簡単なデモンストレーションを実施します。同じようなタイプのマイクロスケール実験装置を購入する場合には IChO 34 のウェブサイトを参考にしてください。
実験問題の試験では火を使う実験は行ないません。その代わりに電気ヒーターを利用する予定です。また,悪臭がしたり危険な薬品を使用する予定もありません。
マイクロスケール実験装置のガラス器具を使うと,通常のスケールのガラス器具により組み立てられるものと同じような装置を組むことができます。コネクター(d)は異なるガラス器具を接続するために利用するものです。ガラスでできた装置の端の部分を互いに接触させ強く押しつけないよう注意してください。マイクロスケールのガラス装置の組み立て例をいくつか次に示します。
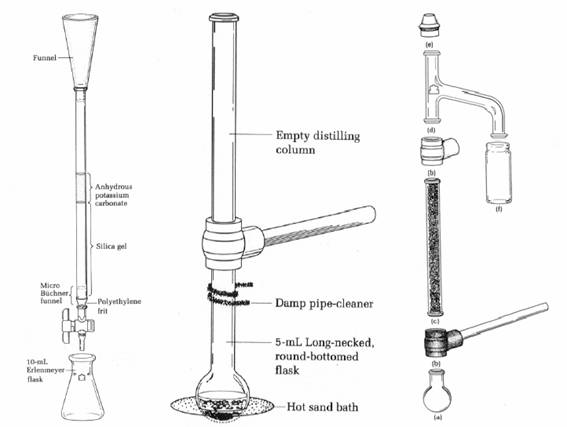
図1 (a) クロマトグラフィー用カラム (b) 還流装置 (c) 分別蒸留装置
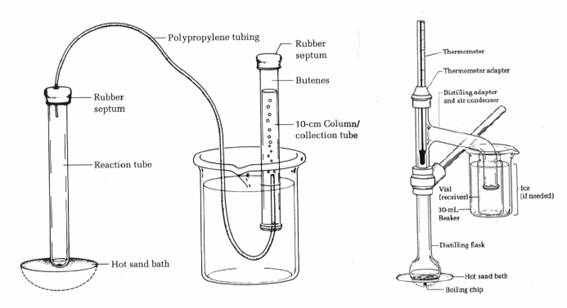
図2 (a) 気体捕集装置 (b) 蒸留装置
フリーデル−クラフツ反応:1,4-ジ-tert-ブチル-2,5-ジメトキシベンゼンの合成
次の反応式は1,4-ジメトキシベンゼンのジ-tert-ブチル化反応を示すものである。
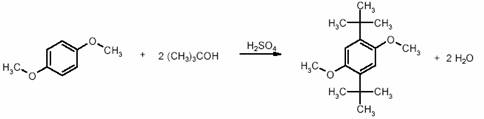
実験操作
50 mL の三角フラスコを用い1,4-ジメトキシベンゼン (360 mg) に氷酢酸 (15 mL)を加え湯浴をもちいてゆっくりと攪拌しながら溶解させる。そこに,フラスコを氷浴中で冷やし,攪拌を続けながらながらtert-ブチルアルコール (0.6 mL) をピペットを用いて加える。続いて,濃硫酸(45滴)を一滴ずつ加える。滴下はパスツールピペットを用いて行ない,一滴落とした毎に,反応液が完全に混合したことを確認してから次の一滴を加えなければならない。反応混合物を次に氷浴から取り除き,徐々に室温まで戻し,さらに25分間攪拌を続ける。反応混合物を再び氷浴を用いて 0 °C まで冷却し,ゆっくりと攪拌しながら水を3滴(非常に注意深く)加えると生成物が結晶化し始める。ここにゆっくりと注意深く氷水(7.5 mL) を加えていくと結晶化が促進される。約10分間放置した後,生成した結晶を吸引ろ過により集める。その生成物を熱メタノール (10 mL) に溶解してから氷浴を用いて冷却することにより再結晶し,再び吸引ろ過により結晶を得る。生成物を空気中で乾燥し,収量を量り,収率を計算,融点を測定する。生成物の純度は薄層クロマトグラフィー;TLC(シリカゲル60, F254 を用い,展開溶媒にはヘキサンを用いる) により求める。このとき,同じTLC プレート上で参照として出発原料も同時に分析する。生成物および出発原料の Rf 値を記録する。このとき,他にも副生成物がある場合にはそれらについても記録しておく。
次のデータを記録せよ。
1 生成物の収量
2 収率(理論収量に対しての%収量)。計算式も示すこと
3 結晶の形状と色
4 融点
5 分析したTLC プレートのコピーとRf 値
必要な薬品
1,4-ジメトキシベンゼン (400 mg)
酢酸 (2.0 mL)
tert-ブチルアルコール (1.0 mL)
濃硫酸 (0.5 mL)
メタノール (10 mL)
水 (20 mL)
TLC プレート(シリカゲル 60, F254)
安全に関する注意: 濃硫酸は,強酸を取り扱う際の安全規則をよく読み,注意して取り扱うこと。硫酸がこぼれて,手や衣服についた場合には即座に水道水を流しながら洗うこと。
問題:
24-1 このアルキル化反応において,求電子剤として作用している化学種は何か
24-2 代わりに1,3-ジメトキシベンゼンを用いた場合の生成物の構造式を示せ
ノート: 融点の測定方法としては何種類かの方法が可能であるが,たとえば,マグネチックスターらーと温度計を備えたシリコーンオイル入りの丸底フラスコを用いる方法,または,コフラー型ブロックを用いる方法などがある。(コフラー型ブロック:温度計やキャピラリー管を入れるための穴の開いた金属製のブロック)またはコフラー型ホットベンチ(可変ヒーターの付属した合金製のプレート)。
マレイン酸の滴定
イントロダクション
マレイン酸は,一段目と二段目の酸が解離するpKa の値がpKa
(1) = 1.8 and pKa (2) = 6.1と大きく異なっているめずらしい化合物である。対照的に,マレイン酸に対応するトランス異性体であるフマル酸は,それぞれのpKa の値は 3.0, 4.4 であり,わずかに違うだけである。この実験では,マレイン酸の一段目および二段目の酸の解離を,異なる指示薬,フェノールフタレイン,メチルオレンジを用いて滴定することにより求める。
マレイン酸 フマル酸
実験操作1
マレイン酸
(290 mg) を5
mL の水に溶かし,フェノールフタレインを2滴加える。その溶液を 1.0 M NaOH
を用いて滴定すると溶液の色が変化して変わらなくなる点がある。
次のデータを記録せよ
1 それまでに用いた1.0 M NaOH の量 (mL)。
2 用いたマレイン酸は何 mmol であるか計算せよ。
3 滴定を開始する前の溶液の色はどうであったか。
4 滴定が完了した後の溶液の色はどうであったか。
実験操作2
マレイン酸(290
mg) を5
mL の水に溶かし,メチルオレンジを2滴加える。その溶液を1.0 M NaOH
を用いて滴定すると溶液の色が変化して変わらなくなる点がある。
次のデータを記録せよ
1 それまでに用いた1.0 M NaOH の量 (mL)。
2 用いたマレイン酸は何 mmol であるか計算せよ。
3 滴定を開始する前の溶液の色はどうであったか。
4 滴定が完了した後の溶液の色はどうであったか。
問題
25-1 滴定の結果をもとに次の指示薬が変化するときのpKa の値を計算せよ。
a フェノールフタレイン b メチルオレンジ
25-2 それぞれのpKa の値が異なるのは次のような理由であると思われる。
□ 分子内で水素結合するため
□ CO2H 基の立体障害
□ シス型ジカルボン酸がトランス型に比べ大きな双極子モーメントをもつため
□ 分子間で水素結合するため
正しい解答をマークせよ。
用いる薬品のリスト
マレイン酸 (600 mg)
1.0 M NaOH (20 mL)
フェノールフタレイン(数滴)
メチルオレンジ(数滴)
2,3-ジフェニルキノキサリンの調製
芳香族化合物につながるシッフ塩基形成の例
2,3-ジフェニルキノキサリンの調製のための反応式は次の通り:
手順
ベンジル(240 mg)とオルト-フェニレンジアミン(IUPAC名:1,2-ジアミノベンゼン)(216 mg)を試験管中で混合し、その混合物を熱水浴で20分加熱する。混合物は始め溶融し、次第に黄褐色の固体へと変わる。この固体を熱メタノール(約10 mL)に溶かし、その溶液を結晶化が始まるまで静置する。もし結晶化が始まらなかったら、再度溶液を温めて、パスツールピペットを使って濁り始めるまで少量の水を加えると結晶化が始まり、室温まで冷やすことで完了する。結晶は生成したらすぐに濾別する。濾別せずに長い間放置しておくと茶色い酸化副生成物が増えてくる。生成物は無色の針状結晶として生成する。重さを計り、収率を計算して、融点を測定しなさい。
次のデータを記録しなさい
1. 生成物の重量
2. 理論収量に対するパーセンテージ表示で生成物の収率(計算も示すこと)
3. 生成物の外観と色
4. 融点
注意
出発原料の1,2-ジアミノベンゼンは着色している場合があり、この実験の前には昇華精製の必要があるかもしれません。
必要な試薬のリスト 安全規範
質問
26-1 ベンズアルデヒドとアニリンの反応における反応式を示しなさい。
3-(4-メトキシフェニル)プロパン酸の合成:接触水素移動反応の例
この水素化反応の化学反応式は下記の通りである。
ギ酸アンモニウムが水素源としてはたらくこの水素化反応は、水素ガスを用いる通常の接触水素化反応の代替法である。どちらの手法でもパラジウム−炭素(活性炭)が触媒として用いられる。
実験操作(下線部は解説を要する操作)
4-メトキシ桂皮酸(IUPAC名:E-3-(4-メトキシフェニル)-2-プロペン酸)(450 mg)を水(7 mL)中に縣濁させ、マグネチックスターラーで撹拌する。これに濃アンモニア水(25%, 0. mL)をゆっくりと滴下する。5分後に、パラジウム(10%)担持活性炭触媒とギ酸アンモニウムを加えた後、混合物を還流下で加熱する。混合物は徐々に透明になる。30分後に(加熱をやめて)反応を停止させる。
反応がどの程度進行したかを薄層クロマトグラフィー(TLC、シリカゲル60 F254)によって調べる。展開溶媒にはヘプタン/酢酸エチル/ギ酸混合溶媒(体積比99:99:2)を用いる。出発物質を基準試料として用いる。もし出発物質が残っていたら、反応混合物をさらに10分間加熱する。
反応混合物を室温まで放冷し、ろ紙を載せたHirsch漏斗でろ過する。漏斗上のろ紙を水(0.5 mLずつ)で4回洗う。透明なろ液に濃塩酸(10 M)で酸性にする(およそ0.5mLでpH 2に達する。pH試験紙を用いること)。白色の沈殿が生じるので、これをHirsch漏斗でろ別する。沈殿は水(10 mL)で洗い、風乾する。
まだ少し湿っている生成物(沈殿)をヘプタン(10 mL)に加え、混合物を還流下で5分間加熱する。そして、得られた無色の溶液をデカンテーション(傾斜ろ過)により別の容器に移す。残渣はヘプタン(5 mLずつ)で2回洗う。ろ液と洗液を集め、固体がすべて溶解するまで加熱する。次に、溶液を砕いた氷浴で冷却し、結晶を析出させる。
得られた結晶をろ別して集め、風乾した後、秤量する。収率を計算し、融点を測定する。
注:この実験は、本冊子の最初に記しているマイクロスケール実験キットを用いれば、1/2のスケール(規模)で行うことができる。
下記のデータを記録しなさい。
1. 生成物の重さ
2. 生成物の収率(理論収量に対する百分率で。計算過程も示すこと)
3. 結晶の形状と色
4. 融点
5. TLCプレートをデータシートに書き写し、各スポットのRf値を計算しなさい。
必要な試薬
4-メトキシ桂皮酸 (500 mg)
アンモニア(25%) (1 mL)
ギ酸アンモニウム (500 mg)
Pd (10% on C) (15 mg)
ヘプタン (20 mL)
酢酸エチル (5 mL)
ギ酸 (0.5 mL)
濃塩酸 (1.0 mL)
TLCプレート(シリカゲル60 F254)
水
問題
27-1 出発物質の量は何mmolか計算しなさい。
27-2 ギ酸アンモニウムは過剰に用いているか?もしそうならその物質量を計算しなさい。
27-3 この水素移動反応プロセスの触媒サイクルはどのようなものか。考えられるものを答えなさい。ヒント:反応中にCO2が発生する。
錯滴定(キレート滴定)
錯滴定による金属イオンの決定例
緒言
EDTA(エチレンジアミン四酢酸)を使った錯形成によってNi2+イオンの濃度を決定する。
EDTAはNi2+と1:1で錯体を作る多座配位子です。指示薬として用いるムレキシドもNi2+と錯体を形成するが、EDTAよりは安定性が低い。この実験の目的は硫酸ニッケル中の結晶水の量を求めることにある。
手順
硫酸ニッケル(約300 mg)を精秤し水に溶かす。100 mLの容量フラスコを用いる。塩化アンモニウム(2.7 g)と濃アンモニア水(17.5 mL)を水(50 mL)に溶解し、緩衝溶液を作る。EDTA標準溶液(0.01 M)をビュレットに入れる。ピペットを使って硫酸ニッケル溶液10.00 mLをエルレンマイヤー(200 mL)に移し、水(約90 mL)で希釈する。エルレンマイヤーを掻き混ぜながら緩衝溶液(10 mL)を加える。少量のムレキシド指示薬を加え、完全に溶解させる。EDTA溶液を使って色(黄色から紫)が変わるまで滴定する。色の変化が遅いときには、少量の濃アンモニア水を滴定の終わりに加える。この実験を二回行う。
次のデータを記録しなさい。
1. EDTAの量をmLで記録する。この溶液の正確な滴定量も記録する。
2. 硫酸ニッケル水和物の重量
3. 溶液中のNi2+の濃度を計算する。
4. 硫酸ニッケル1モル当たりの結晶水のモル数を計算する。
(計算の詳細も示すこと)
必要な試薬のリスト 安全規範
脱塩水?
N-アセチルアラニンの酵素による加水分解:環境に優しいプロセスの例
概要
生体内の反応は酵素の触媒作用により起こる。多くの酵素は非常に選択的な反応を行う。しばしば、ラセミ混合物の一方の鏡像異性体の反応に対して選択的に触媒作用を示す。現代の化学では酵素は試験管内の多くの反応プロセスで使われる。中でも鏡像異性体の一方を純粋な形で合成するために使われることが多い。この実験では、N-アセチルアニリンのアシラーゼIという酵素による加水分解反応について調べる。化学反応式は下記の通りである。
反応の進む様子は、生成するアラニンの量をニンヒドリンとの反応で追跡することにより調べる。化学反応式は次の通りである。
ニンヒドリン インダン-1,2,3-トリオン
アラニン 紫色の陰イオン吸収極大波長λmax = 592 nm
実験操作
N-アセチルアラニンのラセミ混合物(262 nm, 20 mmol)を水(10 mL)に溶かす。かきまぜながら、水酸化リチウム一水和物(84 mg, 2.0 mmol)の水(4 mL)溶液を少しずつ最初の溶液に加える。この溶液のpHが7になるまで、pH試験紙でpHを追跡する。次にこの溶液をかき混ぜながら、アシラーゼI(10 mg)の水溶液(5 mL の水に酵素を加え、ケイソウ土を敷いた小さなガラスフィルターでろ過することにより調製する)を、2分かけて加える。次に、水を加えて体積をちょうど20 mLに調整する。得られた反応混合物は、37℃(水浴中)に60分間保つ。
次に、0.25 mLの溶液を正確に量り取って(注射器または微量用メスピペットを使うこと)試験管に移し、ニンヒドリン(Sigma社N 1632)(1.25 mL)を加える。この溶液を沸騰水中で20分間加熱すると、濃い紫色に発色する。放冷した後、全量を、4 M酢酸リチウム緩衝液(pH = 5.2)とジメチルスルホキシドの1:3混合溶液からなる緩衝液に加え、メスフラスコで250 mL定容にする。次に、分光光度計を用いて、波長λ= 592 nmでの吸光度を測定する。同じ酢酸リチウム−ジメチルスルホキシド混合溶液に溶かしたニンヒドリンを基準試料として用いる。紫色の複合体(陰イオン?)の分子吸光係数はε= 13350 L mol-1cm-1である。
下記のデータを記録しなさい
1.N-アセチルアラニンのラセミ混合物の初濃度
2.λ= 592 nmでの吸光度
3.酵素反応で生成したアラニンの量をmmol単位で計算しなさい。
4.反応率(転化率)を%単位で計算しなさい。
問題
29-1 生成したアラニンは光学的に純粋か(はい/いいえ)?
29-2 反応率が50%より小さい場合、未反応のN-アセチルアラニンは光学活性を持たないか、一方の鏡像異性体が多くなっているか、それとも光学的に純粋か?
29-3 反応率がちょうど50%の場合、上の問題に対する答えはどうなるか?
29-4 反応率が50%を超えることは可能か(はい/いいえ)?
特別課題
もし時間が許すなら、10分後、25分後、40分後および60分後に反応を停止して、それぞれアラニンの濃度を測定してみよ。アラニン濃度を時間に対してプロットしたグラフを作り、最適の反応時間を推定せよ。
必要な試薬
N-アセチルアラニン (265 mg)
アシラーゼI (10 mg)
水酸化リチウム (85 mg)
ニンヒドリン溶液(Sigma社N 1632)(2 mL)
ジメチルスルホキシド (約70 mL) 約200 mL 必要なはず。
酢酸リチウム緩衝液 pH = 5.2 こちらが約70 mLのはず。